Es ist aber wahrscheinlich, dass sich beim Umzug doch das ein oder andere Problem eingeschlichen hat. Bitte meldet Probleme inkl. möglicht genauer Beschreibung und evtl. eines Screenshots an Klaus Schaper.
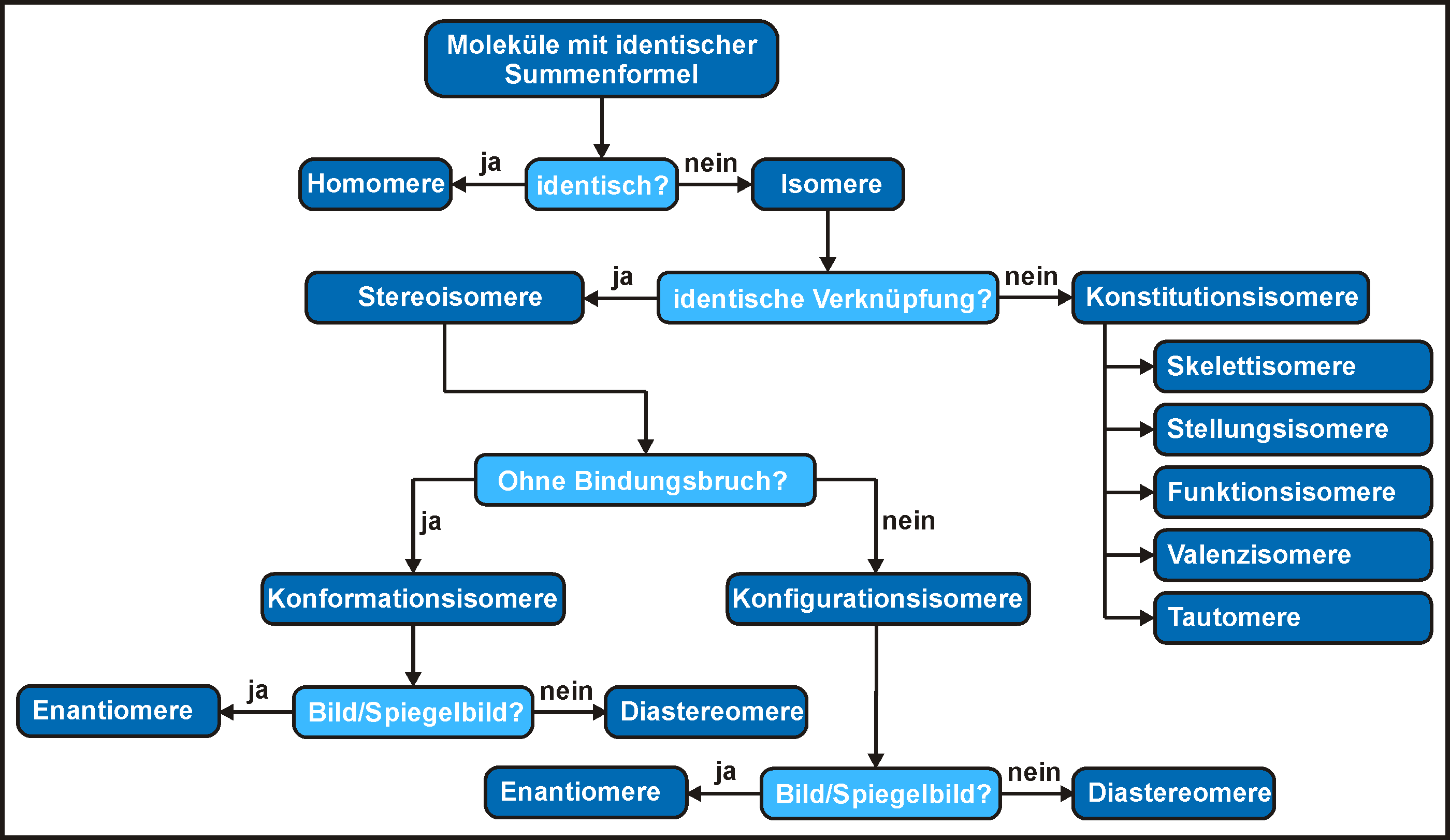
Enthält eine Übersicht über alle wichtigen Isomeriearten
Studienfach:
Alle_Veranstaltungen
Lernziel
Dieses Lernmodul definiert den Begriff der Isomerie und die wichtigsten Arten der Isomerie für den organischen Chemiker. Nach der Bearbeitung des Modules sollen Sie in der Lage sein
- den Begriff Isomerie zu definieren,
- die verschieden Arten der Isomerie zu benennen,
- diese Arten der Isomerie zu definieren und zu erklären und
- in der Lage sein, die Arten der Isomerie an prakischen Beispielen zu erkennen.
Einführung
Die zentralen Begriffe der Isomerie sind im untenstehenden Schema zusammengefasst. Oberhalb des Schemas findet Ihr die dazugehörigen erklärenden Texte. Diese sind so kurz gefasst, dass man die einzelnen Texte und die Abbildung immer gleichzeitig betrachten kann (Zumindest auf einem gängigen PC, auf mobilen Devices kann es Schwierigkeiten geben.)
Bevor wir auf den Inhalt eingehen, kurz einige Hinweise zur Steuerung:
- Mit dem Weiter-Pfeil (rechts unter der nächsten Überschrift) könnt Ihr zur nächsten Textseite naviegieren, mit dem Zurück-Pfeil (links) zur vorherigen Seite.
- Zusätzlich sind die Textseiten durchnummeriert. Durch auswählen der entsprechenden Seitenzahl (unterhalb des nächsten Textblockes) wird zur gewählten Seite geschrollt.
- Alle Textfelder in der Graphik sind interaktiv. Durch Klicken auf ein "Isomeriefeld" (dunkelblau) springt das Modul direkt zur Seite, auf der die entsprechenden Lerninhalte zu finden sind. Durch "hovern" über einem Entscheidungsfeld (hellblau) wird rechts oben in der Abbildung die Frage noch einmal ausformuliert angezeigt.
- Über diese Navigationselemente hinaus gibt es noch die History. Hier kann man durch die letzten besuchten Seiten vorwärts und rückwärts navigieren.
-
In der rechten, grauen Spalte befinden sich unten neben der Abbildung noch drei Button.
- Menü anzeigen: Ein Menü wird angezeigt, welches die schnelle Navigation zu jeder Seite erlaubt. Bei der Auswahl einer Seite wird gleichzeitig "ausrichten" und "Ansicht fixieren" (siehe die nächsten zwei Punkte) durchgeführt.
- ausrichten: Die Darstellung wird so angepasst, dass das Textfeld und die Abbildung optimal in das Browserfenster passen.
- Ansicht fixieren/Fixierung aufheben: Wurde die Seite mit Hilfe von "ausrichten" angepasst, so möchte man die Seite nicht mehr versehentlich aus dem sichtbaren Bereich scrollen. "Ansicht fixieren" verhindert das versehentliche scrollen. Um das Scrollen aus dem eingefrorenenen Bereich hinaus zu aktivieren, muss "Fixierung aufheben gewählt werden."
Tipp: Wenn Sie ein Tablett oder Notebook, nutzen, dann kann es sinnvoll sein, Die Webseite zu zoomen. Bei allen gängigen Browsern können Sie mit "Strg" + "-" die Abbildung und den Text verkleinern und dann noch einmal "ausrichten" wählen.
Einleitung
Betrachten wir zwei beliebige Moleküle, so gibt es prinzipiell zwei Möglichkeiten.
- Die beiden Moleküle haben die gleiche Summenformel.
- Die beiden Moleküle haben verschiedene Summenformeln.
Im zweiten Fall ist die Situation einfach - die beiden Moleküle sind verschieden. Im ersten Fall ist das nicht so klar.
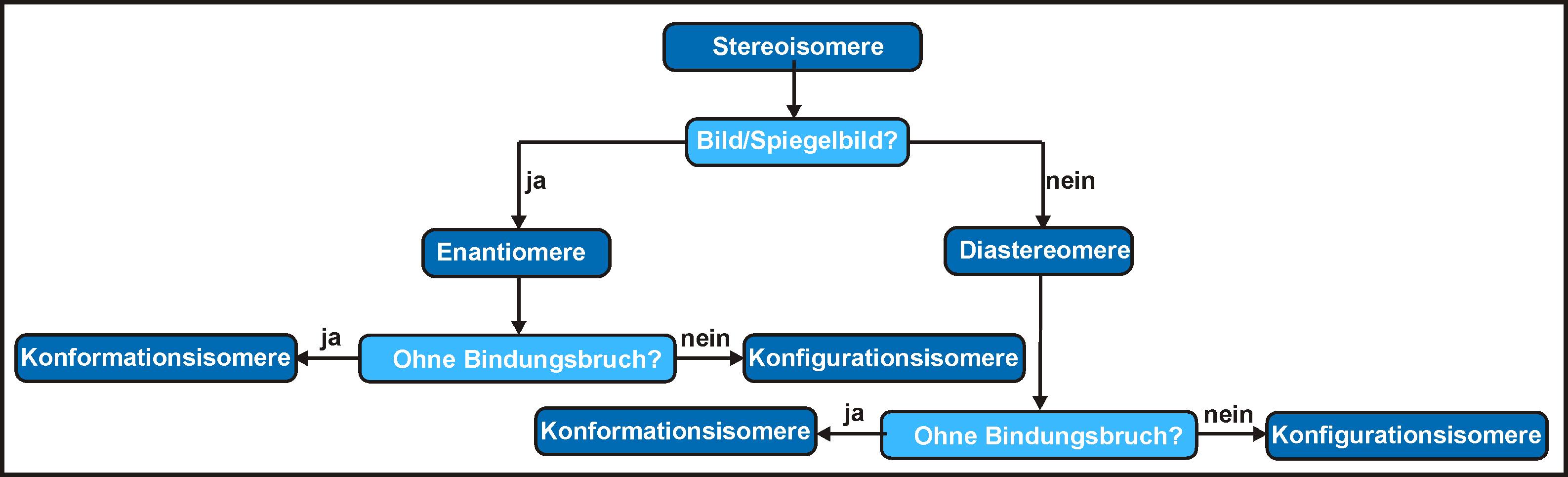
Betrachten wir nun das untenstehende Schema. Wir beginnen oben genau am Punkt 1. Wir haben zwei Moleküle mit identischer Summenformel. Dann stellt sich die Frage, ob die beiden Moleküle identisch sind ("identisch?")? Identisch heißt, dass sich alle Atome der beiden Moleküle zur Deckung bringen lassen!
Homomere
Auf diese Frage gibt es nur zwei Antworten. Im einfachen Fall heißt die Antwort "ja". Die beiden Moleküle sind identisch. Sie lassen sich zur Deckung bringen! Dann nennt man die Moleküle Homomere.
Zwei Moleküle sind Homomere, wenn sie sich vollständig zur Deckung bringen lassen.
Die Alternative ist auf der nächsten Seite dargestellt.
Isomere I
Lassen sich die Moleküle nicht zur Deckung bringen, ist die Antwort also "nein", so liegen Isomere vor.
Zwei Moleküle sind Isomere, wenn sie die gleiche Summenformel haben und sich nicht vollständig zur Deckung bringen lassen.
Für Homomere ist die Betrachtung hier zu Ende, im folgenden werden die verschiedenen Arten der Isomerie diskutiert.
- Die Moleküle A und B sind Homomere, oder
- Molekül A und B sind homomer.
Isomere II
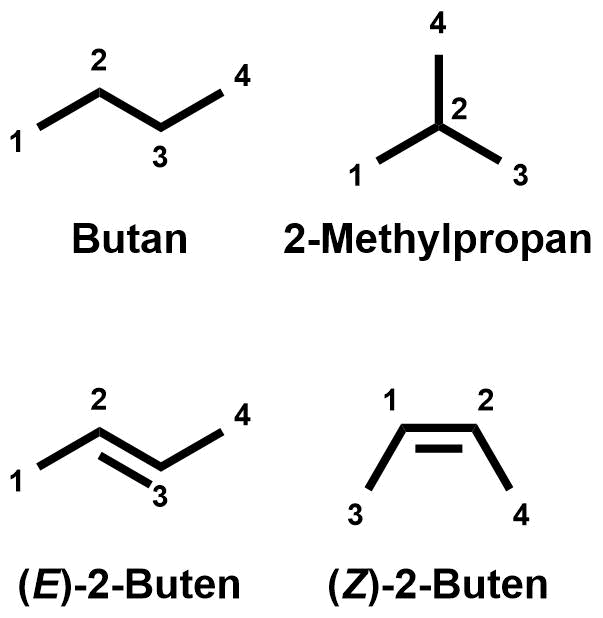
Die erste Frage zur Unterscheidung von Isomeren lautet: "Ist die Verknüpfung der Atome in beiden Isomeren gleich?"
In der Abbildung rechts ist in jeder Zeile ein Isomerenpaar gezeigt. In der ersten Zeile ist die Verknüpfung der Atome verschieden (Atom 4 hängt in der linken Struktur an Atom 3, in der rechten Struktur an Atom 2).
In der zweiten Zeile ist die Verknüpfung der Atome in beiden Strukturen identisch (Atom 4 hängt an Atom 3 hängt an Atom 2 hängt an Atom 1).
Stereoisomere I (Definition)

Wird die Frage "Ist die Verknüpfung der Atome in beiden Isomeren gleich?" mit "ja" beantwortet, so spricht man von Stereoisomeren (zweite Zeile in der Abbildung).
Zwei Isomere sind Steroisomere, wenn die Atome die gleiche Verküpfung aufweisen.
Auf die verschiedenen Arten von Stereoisomeren kommen wir auf Seite 13 noch einmal zurück.
Konstitutionsisomere

Wird die Frage
"Ist die Verknüpfung der Atome in beiden Isomeren gleich?"
mit "nein" beantwortet, so spricht man von Konstitutionsisomeren
(erste Zeile in der Abbildung).
Konstituionsisomere werden im deutschen auch
Verknüpfungsisomere genannt.
Zwei Isomere sind Konstitutionsisomere, wenn die Atome eine unterschiedliche Verküpfung aufweisen.
Auf die verschiedenen Arten von Konstitutionsisomeren gehen wir auf den nächsten Seiten ein.
Skelettisomere
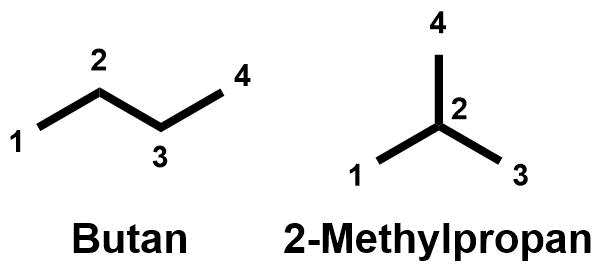
In der Abbildung rechts ist noch einmal das Bild mit den beiden Konstitutionsisomeren von den vorangegangenen Seiten gezeigt. Die beiden Isomere unerscheiden sich in ihrem Kohlenstoffgerüst. Das Kohlenstoffgerüst bildet quasi das Skelett des Moleküls. Daher spricht man hier von Skelettisomeren.
Skelettisomere sind Konstitutionsisomere, die sich in der Verknüpfung des Kohlenstoffgerüstes (des Skelettes) unterscheiden.
Stellungsisomere
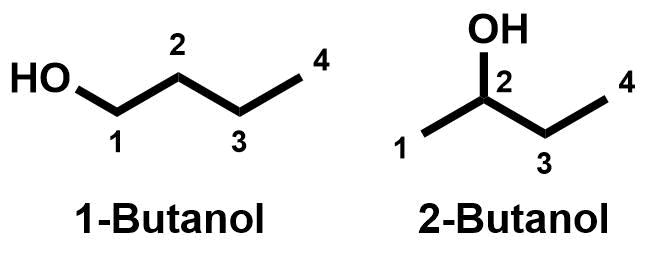
Rechts sind wie auf der vorangegangenen Seite zwei Konstitutionsisomere gezeigt. Diese unterscheiden sich aber im Gegensatz zu den vorherigen Beispielen nicht im Kohlenstoffgerüst (Skelett). Hier ergibt sich der Unterschied durch die Position (Stellung) der funktionellen Gruppe. Hier spricht man von Stellungsisomeren.
Stellungsisomere sind Konstitutionsisomere, die sich in der Position (Stellung) einer funktionellen Gruppe unterscheiden.
Funktionsisomere
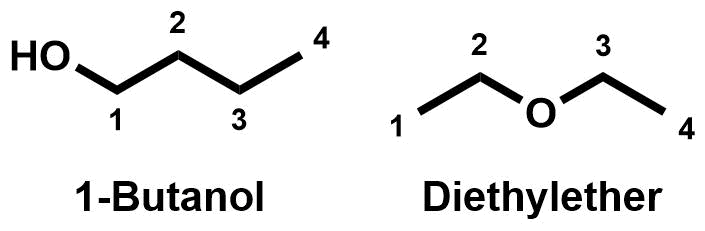
Eine weitere Klasse von Konstitutionsisomeren zeigt die Abbildung rechts. Die beiden Konstitutionsisomeren haben verschiedene funktionelle Gruppen. Links ist ein Alkohol gezeigt, rechts ein Ether. Da sich die beiden Konstitutionsisomere in ihrer Funktionalität unterscheiden, nennt man sie Funktionsisomere.
Funktionsisomere sind im eigentlichem Sinn keine Skelettisomere. Zwar ist auch hier das Kohlenstoffgerüst anders, aber hier sind nicht wie auf Seite 7 vier Atome anders angeordnet, sondern die vier Atome sind in zwei Gruppen a zwei Atome aufgespalten.
Funktionsisomere sind Konstitutionsisomere, die sich in der Art einer funktionellen Gruppe unterscheiden.
Valenzisomere
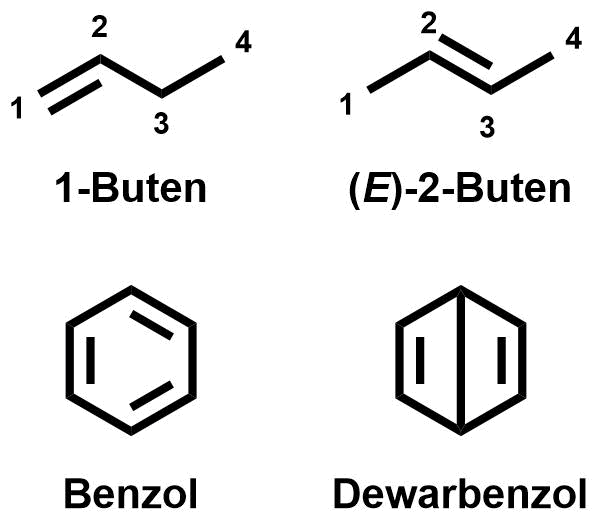
Rechts oben sind wieder zwei Konstitutionsisomere gezeigt (1-Buten und (E)-2-Buten. Sie unterscheiden sich nicht Kohlenstoffgerüst, die Verknüpfung der Kohlenstoffatome ist gleich. Allerdings hat sich die Lage der Doppelbindung verändert. Systeme, die sich durch die Lage von Doppel- und Einfachbindungen unterscheiden, nennt man Valenzisomere.
Auch bei Benzol und Dewarbenzol handelt es sich um Valenzisomere.
Valenzisomere sind Konstitutionsisomere, die sich in der Lage von Einfach- und Doppelbindungen unterscheiden.
Tautomere
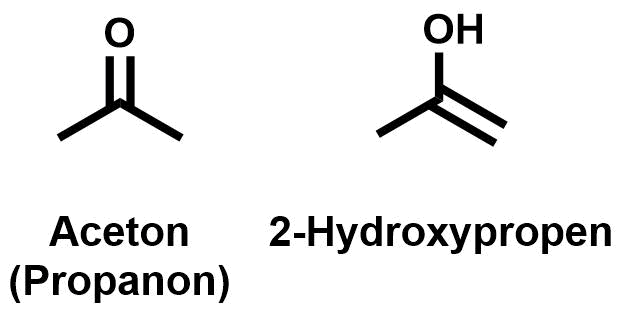
Die letzte Klasse von Konstitutionsisomeren, die hier genannt werden soll, ist rechts gezeigt. Die beiden Strukturen, das Keton (Aceton) und das Enol ((E)-2-Hydroxypropen) sind Funktionsisomere und Valenzisomere, entsprechend den oben gegebenen Erklärungen. Sie entstehen leicht durch Wanderung eines Protons unter Verschiebung von Einfach- und Doppelbindungen. Verbindungen die sich auf diese Art und Weise leicht inernander umwandeln, nennt man Tautomere.
Tautomere sind Konstitutionsisomere, die sich unter Verschiebung einer Gruppe (meist eines Potons) und von Einfach- und Doppelbindungen leicht ineinander umwandeln.
Zusammenfassung
Bei Skelettisomeren, Stellungsisomeren, Funktionsisomeren, Valenzisomeren und Tautomeren handelt es sich jeweils um eine Untergruppe von Konstitutionsisomeren. Es ist durchaus möglich, dass eine Verbindung in mehrere Klassen eingeordnet wird.
In dieser Hinsicht stellt diese Einteilung eine besondere Situation dar. Alle anderen Klassifikationen erfolgen durch strickte ja/nein Antworten, so dass Isomere eindeutig der einen oder anderen Klasse zugeordnet werden können.
Nachdem wir jetzt die Konstitutionsisomere vollständig bearbeitet haben, kehren wir nun zu den Stereoisomeren (siehe Seite 5) zurück.
Stereoisomere II (Einteilung)
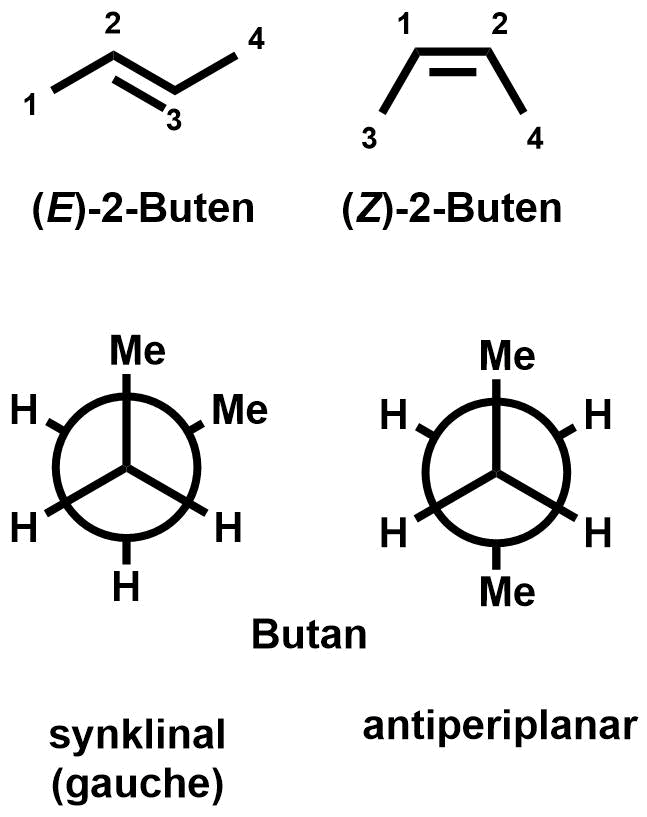
Rechts oben sind zwei Stereoisomere gezeigt. Es handelt sich um (E)-2-Buten und (Z)-2-Buten. Darunter sind zwei stereoisomere Strukturen des Butans gezeigt, die synklinale Form und die antiperiplanare Form (siehe scheLM 3D - Butan). Diese beiden Formen können durch Rotation um eine Einfachbindung ineinander überführt werden. Dies ist für das obere Beispiel nicht möglich.
Zur Unterscheidung von zwei Stereoisomeren stellen wir also die Frage: "Können die beiden Stereoisomeren durch Rotation um eine Einfachbindung ineinander überführt werden?"
Konformationsisomere
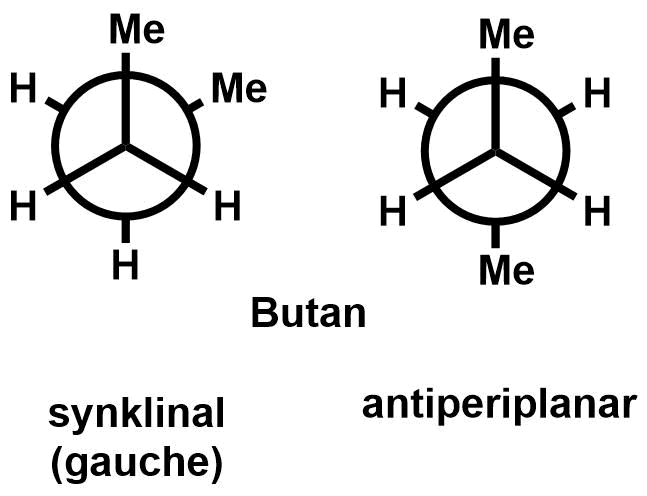
Beantworten wir die Frage: "Können die beiden Stereoisomeren durch Rotation um eine Einfachbindung ineinander überführt werden?" mit "Ja", so handelt es sich um Konformationsisomere. Die beiden rechts gezeigten stereoisomeren Strukturen von Butan können durch Rotation um die zentrale Einfachbindung ineinander überführt werden (siehe scheLM 3D - Butan).
Konformerationsisomere sind Stereoisomere, die durch Rotation um eine oder mehrere Einfachbindungen auseinander hervorgehen.
Im Cyclohexan existieren verschiedene Konformationsisomere (Konformationen), wie z.B. die beiden verschiedenen Sessel, aber auch Wanne (Boot) und Twist (siehe scheLM 3D - Cyclohexan).
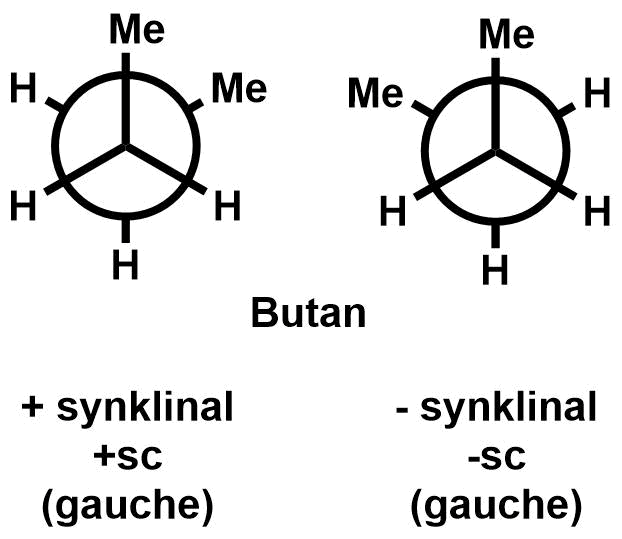
Konformere/Rotamere
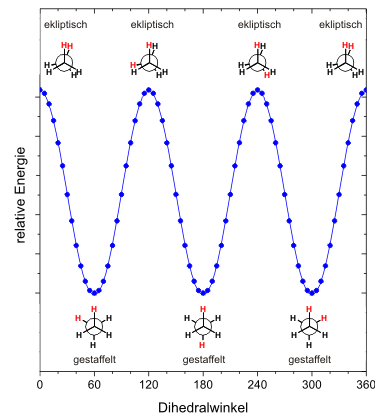
Im Ethan sind zwei Methylgruppen über eine Einfachbindung miteinanderverbunden. Diese beiden Methylgruppen können gegeneinander rotieren und dabei beliebige Anordnungen (Konformationen) annehmen (siehe scheLM 3D - Ethan). Es gibt also beliebig viele Konformationsisomere.
Verschiedene Konformationsisomere haben auch verschiedene physikalische Eigenschaften, und auch verschiedene relative Energien. Die ekliptische Anordnung ist besonders instabil (Maxima auf der Energiehyperfläche), die gestaffelte Anordnung ist besonders günstig (Minima auf der Energiehyperfläche, siehe Abbildung rechts). Die Konformationsisomere in der gestaffelten Anordnung werden auch Konformere oder Rotamere genannt.
Konformationsisomere, die energetisch besonders günstig sind (Minima auf der Energiehyperfläche) werden Konformere oder Rotamere genannt.
Konfigurationsisomere
Zur Einteilung der Stereoisomere hatten wir die Frage gestellt: "Können die beiden Stereoisomeren durch Rotation um eine Einfachbindung ineinander überführt werden?" (siehe Seite 13). Wie wir auf den vorangegangenen Seiten gesehen haben, erhalten wir Konformationsisomere, wenn wir diese Frage mit "ja" beantworten. Beantworten wir die Frage mit "nein", so kommen wir zu den Konfigurationsisomeren. Ein Beispiel ist rechts gezeigt.
Stereoisomere, die sich nicht durch Rotation um eine Einfachbindung ineinander überführen lassen, werden Konfigurationsisomere genannt.
Stereoisomere III (Zusammenfassung)
Stereoisomere werden in Konformationsisomere und Konfigurationsisomere unterteilt. Dazu wird das folgende Kriterium verwendet: "Können die beiden Stereoisomeren durch Rotation um eine Einfachbindung ineinander überführt werden?"
Wichtig: Konformationsisomer und Konfigurationsisomere sind
Stereoisomere! Bevor wir uns die Frage stellen, ob Konformationsisomere
oder Konfigurationsisomere vorliegen, müssen wir die Frage
beantworten,
ob Stereoisomere vorliegen.
Sonst können unsere Schlussfolgerungen falsch sein.
Sowohl Konformationsisomer als auch Konfigurationsisomere können in zwei Klassen von Stereoisomeren unterschieden werden, in Enatiomere und in Diasteromere.
Stereoisomere IV (Enatiomere und Diastereomerer)
Sowohl Konformationsisomere, als auch Konfigurationsisomere werden also in Enatiomere und Diastereomere unterschieden.
Daraus ergibt sich, dass für eine erschöpfende Beschreibung der Stereoisomerie weder das Begriffspaar Konformationsisomere oder Konfigurationsisomere, noch die Beschreibung Enatiomere oder Diastereomere hinreichend ist.
Für eine vollständige Beschreibung werden immer zwei Begriffe benötigt, also
- konfigurationsisomere Enantiomer,
- konfigurationssiomer Diastereomer,
- konformationsisomere Enantiomer oder
- konformationsisomere Diastereomer.
Schauen wir uns nun zunächst die Situation für Konfigurationsisomere an. Wir stellen uns die Frage: "Verhalten sich die beiden Konfigurationsisomere wie Bild und Spiegelbild"
Enantiomere (Konfigurationsisomere)
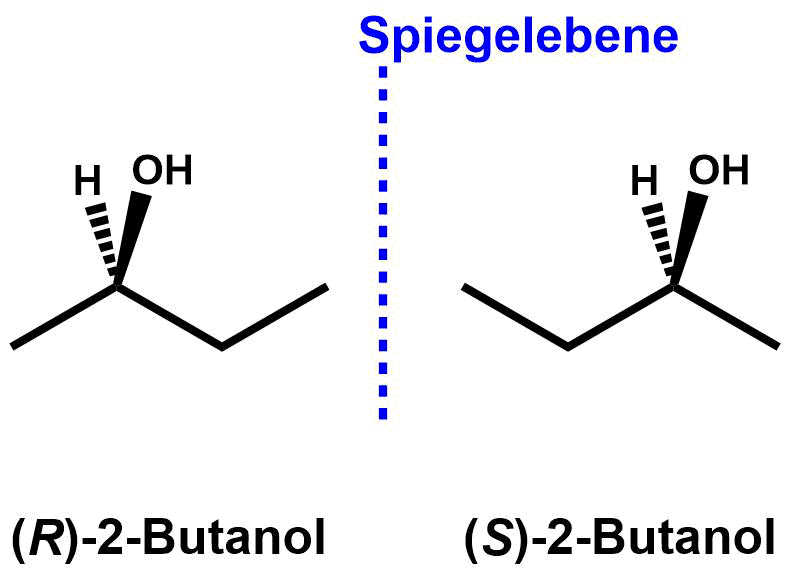
Haben wir zwei Konfigurationsisomere vorliegen (siehe Abbildung rechts) und wir beantworten die Frage: "Verhalten sich die beiden Konfigurationsisomere wie Bild und Spiegelbild" mit "ja", so handelt es sich um Enantiomere.
Verhalten sich zwei Konfigurationsisomere wie Bild und Spiegelbild, so nennt man diese Enantiomere.
Jedes Bild hat genau ein Spiegelbild. Daher treten Enantiomere immer paarweise auf. Ein typisches Beispiel für ein Enantiomerempaar im Bereich der Konfigurationsisomere ist ein Molekül mit einem Sterozentrum.
Diastereomere (Konfigurationsisomere)

Wie wir gerade gesehen haben, nennt man zwei Konfigurationsisomere, die sich wie Bild und Spiegelbild verhalten Enantiomere. Beantworten wir die Frage: "Verhalten sich die beiden Konfigurationsisomere wie Bild und Spiegelbild" mit "nein", so handelt es sich um Diastereomere.
Verhalten sich zwei Konfigurationsisomere nicht wie Bild und Spiegelbild, so nennt man diese Diasteromere.
Eine Struktur kann immer nur ein Enantiomer besitzen, aber sie kann mehrere Diastereomere haben.
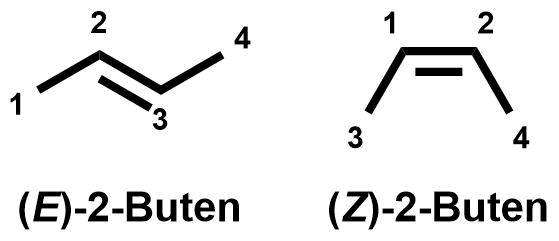
Ein typisches Beispiel für Diasteromere ist rechts gezeigt. Die E-/Z-Isomerie (cis-/trans-) an einer Doppelbindung führt zu Diastereomeren.
Diastereomere (Konfigurationsisomere, weitere Beispiele)
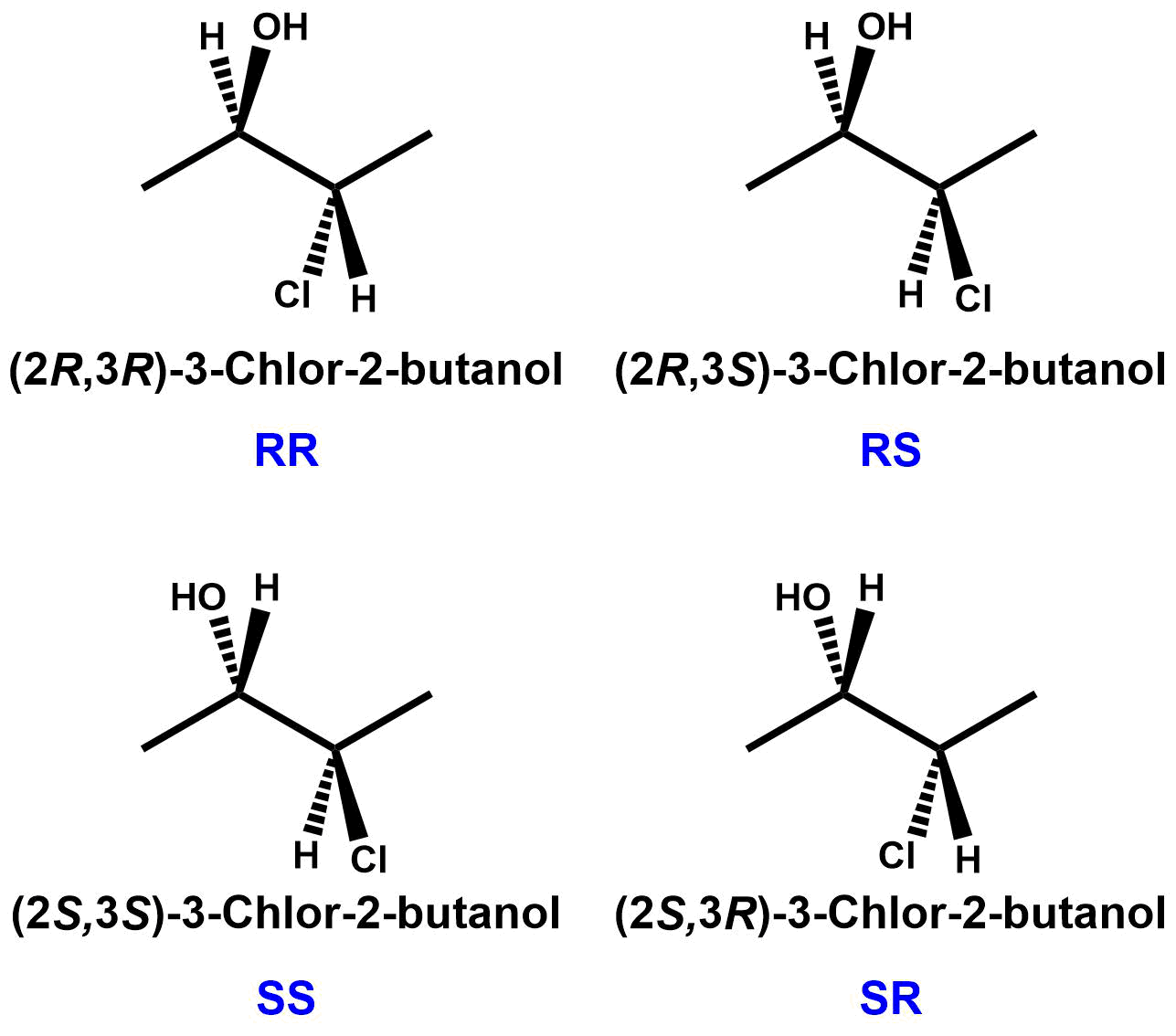
In der Abbildung auf der rechten Seite sind vier Konfigurationsisomere gezeigt. Es handelt sich um ein Molekül mit zwei Stereozentren. Allgemein kann ein Molekül mit n Stereozentren 2n Konfigurationsisomere besitzen (wenn es sonst keine stereogenen Einheiten besitzt). In diesem Fall also 22 = 4. Es sind also alle möglichen Konstitutionsisomeren abgebildet.
Oben links ist das RR-Isomer gezeigt, darunter befindet sich das SS-Isomer. Beide Stereozentren sind umgedreht und es handelt sich um Bild und Spiegelbild, also um ein Enantiomerenpaar. Die anderen beiden Isomere (RS und SR) sind diastereomer sowohl zu RR, als auch zu SS.
RS und SR bilden wiederum ein Enantiomerenpaar.
Wichtig: Bei dieser Diskussion wurde die Tatsache, dass alle vier Konfigurationsisomere in verschiedenen Konformationen vorliegen können, vernachlässigt. Die Kette ist immer in einer Zick-Zack-Anordnung gezeigt.
Diastereomere (Konfigurationsisomere, Mesoform I)
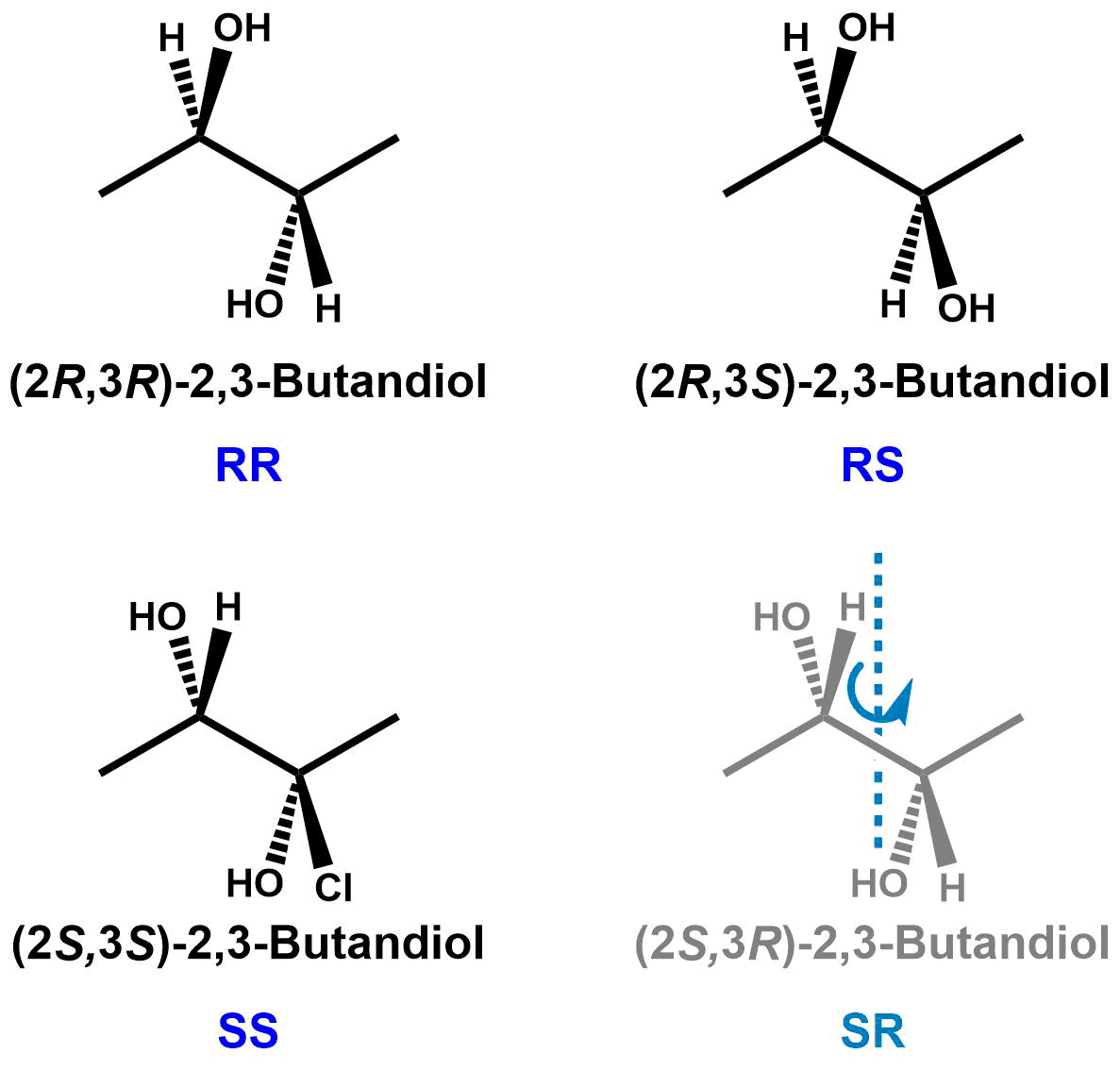
Wie auf der vorangegangenen Seite haben wir wieder Moleküle mit zwei Stereozentren. Daher sollte es wieder vier Konfigurationsisomere geben. Wie im vorangegangenen Beispiel gibt es ein Enantiomerenpaar bestehend aus der RR- und der SS-Form. Auch zur RS-Form findet sich ein Spiegelbild in unserer Abbildung, die SR-Form. Diese ist aber nicht das Enantiomer zu RS. Dies ist zunächst überraschend.
Schauen wir uns die Situation noch einmal genauer an. In SR gibt es eine zweizählige Drehachse (hellblaue gestrichelte Linie). Diese legt in der Papierebene. Durch Drehung um diese Achse wird SR in RS überführt. SR und RS sind also identisch, es handelt sich um Homomere, nicht um Isomere. Daher ist diese Struktur in grau gezeigt.
Diastereomere (Konfigurationsisomere, Mesoform II)

Da es sich bei den Strukturen SR und RS nicht um Isomere handelt, können die Begriffe Stereoisomer, Konfigurationsisomer, Enantiomer und Diastereomer hier nicht angewendet werden!
In diesem Fall gibt es statt der vier möglichen nur drei verschiedenen Isomere. Die Struktur RS ist mit Ihrem Spiegelbild identisch. Eine solche Struktur wird als Mesoform bezeichnet.
Ein Molekül, welches Stereozentren besitzt und mit seinem Spiegelbild identisch ist, wird als Mesoform bezeichnet.
Enantiomere (Konformationsisomere)
Hier ist die Diskussion der Konfigurationsisomerie abgeschlossen und wir kehren zu den Konformationsisomeren (siehe Seite 14) zurück.
Wie schon auf Seite 18 erläutert, können Konformationsisomere genau wie Konfigurationsisomere in Enantiomere und Diastereomere unterschieden werden.
Rechts oben sind zwei Konformationsisomere des Butans gezeigt. Diese beiden Konformationsisomere verhalten sich wie Bild und Spiegelbild, die beiden Stukturen sind also verschieden. Es handelt sich also um enantiomere Konformationsisomere.
Diastereomere (Konformationsisomere)

Rechts ist das Bild von Seite 14 (Konformationsisomere) noch einmal wiederholt. Es handelt sich um zwei Konformationsisomere, also Stereoisomere, die sich durch Rotation um eine Einfachbindung ineinander überführen lassen. Die beiden Strukturen verhalten sich nicht wie Bild und Spiegelbild, sie sind diastereomere Konformationsisomere.
Zusammenfassung
Liegen Moleküle mit identischer Summenformel vor, so können diese durch eine Reihe von Ja/Nein-Fragen klassifiziert werden.
Konstituionsisomere lassen sich dabei in verschiedene Klassen einteilen. Dabei können zwei Konstitutionsisomere in mehrere der Unterklassen passen.
Für Stereoisomere ist die Situation etwas anders. Hier erfolgt die Klassifizierung durch zwei weitere Ja/Nein-Fragen. Zur vollständigen Beschreibung von Stereoisomeren muss die Klassifizierung in zwei Begriffspaare erfolgen: "Eantiomer/Diastereomer" und "Konformationsisomer/Konfigurationsisomer".
alternativer Stammbaum
Wir haben Stereoisomere zunächst in Konformationsisomere und Konfigurationsisomere unterschieden, um diese dann jeweils in Enantiomere und Diastereomere zu unterscheiden.
Diese Unterscheidung kann auch in umgekehrter Reihenfolge erfolgen (Alternativer Stammbaum). Stereoisomere werden zunächst in Enantiomere und Diastereomere unterschieden, und diese dann in Konformationsisomere und Konfigurationsisomere.
Egal welche Reihenfolge man wählt, das Ergebnis ist das gleiche und zur Beschreibung sind zwei Isomeriebegriffe erforderlich.
Alternativer Stammbaum
Header 28
...
Header 29
...
Header 30
...
scheLM 3D
scheLM Gl
scheLM I4
scheLM IR
scheLM n2s
scheLM NMR
scheLM PSE
scheLM ReRe
scheLM TV
scheLM tys
scheLM Vote
Auszeichnungen Personen Datenschutz Impressum
Wir danken dem eLearning-Förderfonds der Heinrich-Heine-Universität und dem Lehrförderungsfond der Heinrich-Heine-Universität, sowie dem Fellowship Digitale Innovation in der Hochschullehre des Landes Nordrhein-Westfalen, sowie OER-Content.NRW für die Unterstützung.
© Copyright 2013 bis 2025, PD Dr. Klaus Schaper


